Milad Manafi
Departamento de Ciencia Animal, Facultad de Ciencias Agrícolas,
Universidad de Malayer, Malayer, Irán.
[email protected]
En general, las diferentes especies de aves de corral requieren un suministro adecuado de carbohidratos, proteínas, grasas/aceites, vitaminas, minerales y agua (Manafi et al., 2011).
 Sin embargo, un mal manejo y almacenamiento de las materias primas, así como unas elevadas tasas de carbono y humedad en los cebaderos, pueden conducir a una dieta final contaminada con hongos y micotoxinas (Döll y Dänicke, 2004). Sin embargo, un mal manejo y almacenamiento de las materias primas, así como unas elevadas tasas de carbono y humedad en los cebaderos, pueden conducir a una dieta final contaminada con hongos y micotoxinas (Döll y Dänicke, 2004). |

Las micotoxinas son reconocidas como metabolitos tóxicos secundarios producidos principalmente por varias especies de hongos toxigénicos del Aspergillus, Fusarium y Penicillium (Egbontan et al., 2017).
El tipo de micotoxina, el nivel y la frecuencia de exposición (aguda o crónica), el índice de masa corporal, el sexo, los problemas de salud concomitantes y los posibles efectos sinérgicos de otras sustancias químicas afectan a la manifestación de la enfermedad (Manafi et al., 2009).
En las aves de corral, la magnitud de los efectos de estas micotoxinas depende de su presencia en los alimentos y piensos por encima de los límites reglamentarios.
Los diferentes síntomas en las aves de corral y otros animales han sido bien documentados por muchos investigadores:
 Pérdida de peso, anorexia y disminución de la capacidad de conversión alimentaria
Pérdida de peso, anorexia y disminución de la capacidad de conversión alimentaria Inmunosupresión y falta de respuesta a la vacunación
Inmunosupresión y falta de respuesta a la vacunación Baja fertilidad
Baja fertilidad Disminución de la producción de huevos y alta probabilidad de manchas de sangre en los huevos
Disminución de la producción de huevos y alta probabilidad de manchas de sangre en los huevos Agrandamiento de los riñones
Agrandamiento de los riñones Hígado graso pálido y hepatitis
Hígado graso pálido y hepatitis Erosiones en la molleja y lesiones orales
Erosiones en la molleja y lesiones orales Mayor incidencia de malformaciones en las patas
Mayor incidencia de malformaciones en las patas Aumento de la tasa de mortalidad y de las hemorragias viscerales
Aumento de la tasa de mortalidad y de las hemorragias viscerales Reducción de la altura de las vellosidades
Reducción de la altura de las vellosidades
(Alexandros and Jean, 2002; Döll et al., 2004; Jaynes et al., 2007; Marin et al., 2013; Mishra et al., 2013; Manafi et al., 2014; Manafi et al., 2015; Fowler et al., 2015; Manafi et al., 2016; Ji et al., 2016; Manafi, 2018; Manafi et al., 2019, Raj et al., 2021).
Además, existe una alta probabilidad de transferencia de micotoxinas a los subproductos comestibles derivados de las aves de corral alimentadas con piensos contaminados (Figura 1). Este fenómeno puede provocar cáncer, ya que la Organización Mundial de la Salud (OMS) y el Centro Internacional de Investigaciones sobre el Cáncer (IARC) reconocen la carcinogenicidad de algunas micotoxinas (Ganesan et al., 2021).
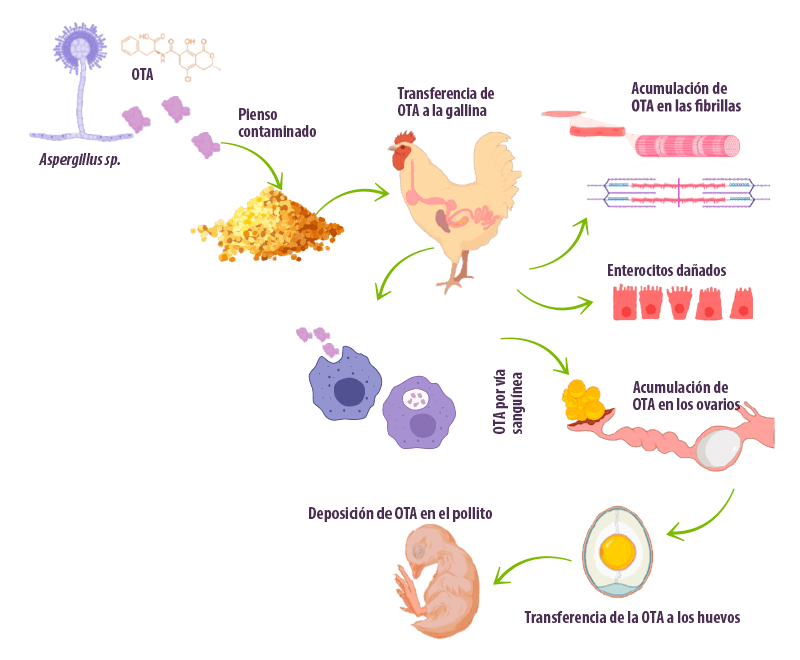
Figura 1. Representación esquemática de la transferencia de Ocratoxina A (OTA) desde el alimento a varias partes de la gallina (adaptado de Ganesan et al., 2021).
|
Los métodos de análisis de micotoxinas más comunes son.
|
 El ELISA es una prueba rápida con una precisión fiable en sustratos sencillos, como los ingredientes crudos de los piensos.
El ELISA es una prueba rápida con una precisión fiable en sustratos sencillos, como los ingredientes crudos de los piensos.
 Por su parte, los análisis basados en HPLC y LC-MS/ MS son relativamente más precisos que los kits de pruebas rápidas y se utilizan para evaluar los eliminadores de micotoxinas, especialmente en sustratos complejos, como los piensos formulados (Niderkorn et al., 2007)
Por su parte, los análisis basados en HPLC y LC-MS/ MS son relativamente más precisos que los kits de pruebas rápidas y se utilizan para evaluar los eliminadores de micotoxinas, especialmente en sustratos complejos, como los piensos formulados (Niderkorn et al., 2007)
La mayoría de las micotoxinas son compuestos liposolubles que pueden ser fácilmente absorbidos desde el lugar de exposición (tracto gastrointestinal o respiratorio) hacia el sistema circulatorio, llegando al hígado donde son metabolizados por el sistema microsomal en metabolitos activos o detoxificados y distribuidos por todo el organismo (Haschek et al., 2002).
A través de los procesos celulares naturales de transcripción y traducción, las mutaciones pueden manifestar o incluso exacerbar la desregulación del crecimiento celular (Manafi et al., 2012)

CONTROL DE MICOTOXICOSIS
Los investigadores están realizando grandes esfuerzos para desarrollar productos rentables y seguros para lograr la descontaminación y remediación de diferentes micotoxinas (preventiva o curativa) en los piensos (Manafi et al., 2019).
Preferiblemente, el nivel de aflatoxinas en los piensos debería ser cero. En cualquier caso, algunas organizaciones reguladoras han establecido su umbral como nivel máximo para las aves de corral.
 Actualmente, la forma más eficaz de proteger a los animales contra la micotoxicosis es la inclusión de adsorbentes en los piensos (Ditta et al., 2018) Actualmente, la forma más eficaz de proteger a los animales contra la micotoxicosis es la inclusión de adsorbentes en los piensos (Ditta et al., 2018) |
La capacidad de los adsorbentes de micotoxinas para eliminar las toxinas se determina mediante ensayos in vitro e in vivo con sus ventajas e inconvenientes específicos.
⇰ En el caso de los estudios in vivo, para obtener resultados consistentes hay que realizar bioensayos específicos.
⇰ En cambio, los experimentos in vitro son relativamente fáciles de realizar, y pueden acortar el tiempo y el coste de la experimentación.

Teniendo en cuenta que el objetivo final de un estudio in vitro es reemplazar los experimentos in vivo en la práctica, las condiciones de los experimentos in vitro deben estar estrechamente controladas y bien diseñadas para obtener registros de investigación precisos (Hahn et al., 2015).
| Sobre esta base, a continuación, se detallan los métodos Físicos y Orgánicos para controlar las micotoxinas en los piensos para avicultura, haciendo hincapié en los experimentos de investigación realizados anteriormente. |
Métodos Físicos
La extracción de micotoxinas, de los piensos es una herramienta eficaz, ya que estos metabolitos secundarios son muy solubles en disolventes orgánicos. La utilización de adsorbentes que fijan las micotoxinas es el método físico más aplicado para proteger a los animales frente a la micotoxicosis.
Las arcillas suelen estar formadas por dos o más capas de óxido mineral y algunas de sus partículas pueden absorber la humedad y expandirse. Sin embargo, su eficacia depende de la estructura química del adsorbente y de la micotoxina, ya que es importante garantizar que los adsorbentes no eliminen nutrientes esenciales de la dieta (Manafi et al., 2012).
| Las zeolitas, los carbones activados y el aluminosilicato cálcico hidratado se encuentran entre las arcillas más importantes utilizadas para controlar la micotoxicosis. Aunque estos métodos son comparativamente caros, su eficacia es parcialmente eficiente. |
Zeolitas
Las zeolitas son compuestos cristalinos de aluminosilicato.
Se registró una mejora del 29-41% en la ganancia de peso corporal en broilers expuestos a 3,50 ppm de aflatoxina (AF) mediante la suplementación dietética de zeolita comercial (Duarte y Smith, 2005).
Muchos otros investigadores han tratado de mitigar los efectos adversos de las micotoxinas en diferentes animales utilizando zeolita (Daković et al., 2005; Dhanasekaran et al., 2011; Rajendran et al., 2020; Raj et al., 2021).

Aluminosilicato cálcico hidratado (HSCAS)
El HSCAS, un filosilicato derivado de la zeolita natural, es quizás el adsorbente de micotoxinas más ampliamente investigado.
Phillips et al. (1988) demostraron que el HSCAS tiene una alta afinidad por la AFB1 después de examinar 38 adsorbentes diferentes que eran representativos de la principal clase química de alúminas, sílices y aluminosilicatos.
Hay una amplia gama de eficacia observada en diferentes estudios que incorporan HSCAS en las dietas para reducir la toxicidad de AF, OTA, y la toxina T-2 en las aves de corral (Huff et al., 1992; Jindal et al., 1993; Kubena et al., 1998; Raju y Devegowda, 2000; Huwing et al, 2001; Girish y Devegowda, 2004; Duarte y Smith, 2005; Khatoon et al., 2018; Wei et al., 2019).

Carbon activado
El carbón activado es un polvo insoluble formado a través de la pirólisis de diferentes tipos de materiales orgánicos y es bastante eficaz para adsorber OTA.
Diferentes estudios han reportado una mejora en el peso corporal de los pollos de engorde tras la inclusión de carbón activado en dietas que contienen diferentes micotoxinas (Ramos y Hernández, 1997; Solfrizzo et al., 2001; Huwing et al., 2001; Duarte y Smith, 2005; Mgbeahuruike et al., 2018).
Bentonita
La bentonita es una arcilla mineral con la característica singular de hincharse hasta varias veces su volumen original cuando se introduce en el agua. Debido a su contenido en montmorillonita, las bentonitas forman geles tixotrópicos como resultado de su capacidad de intercambio de iones.
La bentonita forma un complejo con la toxina, impidiendo la absorción de micotoxinas, como las aflatoxinas, a través del epitelio intestinal (Duarte y Smith, 2005).
Los materiales arcillosos pueden unirse a moléculas de determinados tamaños y configuraciones y se han utilizado eficazmente para disminuir los efectos de las dietas contaminadas con aflatoxinas en las aves de corral. En este sentido, existen multitud de publicaciones que hablan de la descontaminación de micotoxinas en aves de corral (Unsworth et al., 1989; Smith y Ross, 1991; Hagler et al., 1992; Santurio et al., 1999; Rosa et al., 2001; Vieira, 2003; Eralsan et al., 2005; Eraslan et al., 2006; Murugesan et al., 2015; Mgbeahuruike et al., 2018).

Métodos orgánicos
En esta categoría de herramientas de control de micotoxinas, se repasa la aplicación de agentes antioxidantes de origen vegetal, vitaminas, algas, enzimas, manipulación nutricional y métodos biológicos.
Agentes antioxidantes de origen vegetal
Se ha demostrado que la aplicación de algunos extractos derivados de plantas, como la cúrcuma (Curcuma longa) el ajo. (Allium sativum) y la asafétida (Ferula asafetida), contrarrestan la aflatoxicosis en las aves de corral gracias a su actividad antioxidante al reducir el nivel de radicales libres (Manafi et al., 2018).
El sistema antioxidante del cuerpo involucra principalmente agentes reductores (tocoferol, ácido ascórbico, glutatión, carotenoides), peroxidasas (glutatión peroxidasa, catalasa), enzimas (peptidasas, proteasas, vitamina A) y superóxido dismutasa (Renzulli et al., 2004).
Los grupos químicos funcionales más comunes con propiedades de eliminación de radicales son los hidroxilos (fenólicos), los sulfhidrilos (cisteína, glutatión) y los grupos aminos (ácido úrico, espermina) (Lee et al., 2001).


Existen varios estudios sobre el uso de diversos extractos de hierbas para combatir la micotoxicosis en diferentes animales que podrían aliviar parcialmente algunos efectos negativos:
- ⇰ Aumento de peróxidos
- ⇰ Reducción de las actividades enzimáticas antioxidantes
- ⇰ Inhibición de la síntesis de proteínas/ADN
- ⇰ Supresión de la aberración cromosómica
- ⇰ Inhibición de la bioactivación del citocromo P450 de la AFB1
- ⇰ Reducción de los biomarcadores antioxidantes (glutatión peroxidasa y superóxido dismutasa)
- ⇰ Inhibición de la mutagenicidad de la AFB1 y aumento de la formación de aductos AFB1-ADN
(Iqbal et al., 1983; Nyandieka et al.,1990; Surai; 2001; Weiss, 2002; Gowda and Ledoux, 2008; Gowda et al., 2008; Dalleau et al., 2008; Ruan et al., 2019).
Vitaminas
Existen estudios sobre la regeneración del α-tocoferol al reaccionar con otros agentes reductores como el glutatión, el urato (Kagan y Tyurina, 1998) y el ascorbato (May et al., 1998).
Chow (2001) señaló que el α-tocoferol es la forma biológicamente más activa, ya que elimina rápidamente los radicales peroxi al formar un radical tocoferoxi estable y actuar como modificador biológico.
⇰ El pretratamiento con vitamina E redujo significativamente la peroxidación lipídica inducida por AFs (Verma y Nair, 2004).
Entre las vitaminas, el ascorbato (vitamina C) es muy importante debido a su capacidad para eliminar el superóxido, el peróxido de hidrógeno, los radicales de hidrógeno, el ácido hipocloroso y el oxígeno singlete (Chow, 2001).
La riboflavina también tiene una acción protectora frente al daño del ADN inducido por la AFB1 en ratas (Gowda y Ledoux, 2008).
Muchos otros estudios han demostrado los efectos de diferentes vitaminas en animales cuando son expuestos a micotoxinas (Nyandieka et al., 1990; Coelho, 1996; Hoehler y Marquardt, 1996; Diaz y Smith, 2005; Kabak, 2009; Wayne, 2012; Murugesan et al., 2015).


Algas (Spirulina platensis)
El valor nutricional de algunas algas como Spirulina platensis es extremadamente alto.
La espirulina es rica en aminoácidos, vitaminas, ácido gamma-linoleico, azúcares y oligoelementos (EFSA FEEDAP Panel, 2016).
Raju et al., (2004); Abdel-Wahhab y Aly (2005); Dal Bosco et al., (2008); Manafi et al., (2009); Manafi, (2011); Manafi et al., (2012) y Park et al., (2018) también han señalado que Spirulina platensis es eficaz frente a la aflatoxicosis.
Enzimas
Los reactivos de degradación enzimática se utilizan para la biodegradación de la estructura química tóxica de las micotoxinas en metabolitos no tóxicos mediante el uso de microorganismos y sus metabolitos o componentes específicamente extraídos.
Se cree que rompen el grupo atómico funcional de la molécula de la micotoxina, convirtiéndola así en no tóxica (Kabak et al., 2006).
Algunas enzimas, como la carboxiesterasa presente en la fracción microsomal del hígado, la esterasa y la epoxidasa, se están probando para comprobar su aplicabilidad práctica en condiciones de campo (Pasteiner, 1997).
La eficacia demostrada del uso de enzimas frente a la micotoxicosis está bien documentada por numerosos investigadores (Vekiru et al., 2010; Ji et al., 2016; Tso et al., 2019; Fruhauf et al., 2019).


Manipulación nutricional
El aumento del nivel de proteínas en la dieta y la suplementación con L-fenilalanina han demostrado ser eficaces frente a la aflatoxicosis y la ocratoxicosis. Además, el aumento de la suplementación de riboflavina, piridoxina, ácido fólico y colina ha demostrado tener un efecto protector frente a la aflatoxicosis (Ehrich et al., 1986).
Los antioxidantes, como la β-naptoflavona, la vitamina C y la vitamina E, ofrecen protección contra la genotoxicidad inducida por AFs en la mayoría de los estudios in vitro (Johri et al., 1990).
Devegowda et al., (1998); Krska et al., (2008); Bryden, (2012), y Marin et al., (2013) han informado de que la suplementación adicional de las dietas avícolas con micronutrientes puede mitigar parcialmente los efectos adversos de las micotoxinas.
Métodos biológicos
La rápida evolución de la industria de los piensos ha abierto nuevas posibilidades mediante la degradación de las micotoxinas por parte de los microorganismos (Alexandros y Jean, 2002).
Varias levaduras, mohos y cepas bacterianas poseen la capacidad de destruir o transformar las micotoxinas con éxito (Edlayne et al., 2009).
| En esta categoría, se revisarán las degradaciones bacterianas, de protozoos, de hongos y de levaduras. |
DEGRADACIÓN BACTERIANA
Varias especies bacterianas han demostrado su capacidad para degradar AFs (Kong et al., 2012).
Específicamente, en diferentes estudios se ha encontrado que algunas bacterias productoras de ácido, como Lactobacillus plantarum y Lactobacillus acidophilus detoxifican AF, OTA, toxina T-2 y zearalenona (ZEN) (Linderfelser y Ceigler, 1970; Bata y Lásztity, 1999; Turbic et al, 2002; Lahtinen et al., 2004; Kusumaningtyas et al., 2006; Niderkorn et al., 2007; Wu et al., 2009; Kolossova y Stroka, 2009; Rawal y Roger, 2010; Ma et al., 2012; Mishra et al., 2013; Fan et al., 2013 y Fan et al., 2015).

DEGRADACIÓN PROTOZOARIA
Los protozoos son agentes importantes para la biodegradación de micotoxinas en el rumen (Upadhaya et al., 2010).
La mayoría de los estudios sobre el tema indican que la degradación de las micotoxinas se logra, principalmente, por los protozoos ruminales (Jouany et al., 2009). Además Hussein y Brasel (2001) señalaron que hasta el 90% de la degradación de la toxina T-2 se lograba mediante protozoos ruminales.
Tetrahymena pyriformis, a una dosis de 22x106 células, desintoxicó la AFB1 convirtiéndola en sus productos hidroxilos hasta un 5% en 24 horas y un 67% en 48 horas (Robertson et al., 1970).
Se observó que el líquido ruminal intacto que contenía varios protozoos metabolizaba la toxina T-2 y la OTA, mientras que no se observó ningún efecto sobre la AF (Kiessling et al., 1984). Sin embargo, el hecho de que los protozoos no puedan cultivarse in vitro limita la comprensión de su capacidad para degradar micotoxinas (Chaucheyras-Durand y Ossa, 2014; Newbold et al., 2015).
 Los estudios que implican enfoques independientes de los cultivos y que se basan en el análisis de determinados genes y genomas potencialmente asociados a la degradación de las micotoxinas pueden ayudar a mejorar nuestra comprensión del papel de los protozoos en el proceso (Garai et al., 2021). Los estudios que implican enfoques independientes de los cultivos y que se basan en el análisis de determinados genes y genomas potencialmente asociados a la degradación de las micotoxinas pueden ayudar a mejorar nuestra comprensión del papel de los protozoos en el proceso (Garai et al., 2021). |

DEGRADACIÓN FÚNGICA
Se ha descubierto que una sustancia intracelular es la responsable de que A. flavus y A. parasiticus degraden las toxinas formadas en un cultivo cuando su micelio se somete a fragmentación.
Las enzimas peroxidasas producidas por el micelio fúngico, que pueden catalizar el peróxido de hidrógeno en radicales libres, reaccionan con las micotoxinas (Dvorak, 1989; Alexandros y Jean, 2002; Edlayne et al., 2009).

DEGRADACIÓN MEDIANTE LEVADURAS
La irrupción de la biotecnología en la última década ha abierto una nueva vía para abordar el problema de la micotoxicosis mediante el uso de extractos de levadura.
La levadura es una rica fuente de numerosas vitaminas y ciertas especies y cepas pueden detoxificar las micotoxinas mediante su degradación (Biernasiak et al., 2006).
El mananoligosacárido (MOS) derivado de la pared celular de Saccharomyces cerevisiae parece tener una gran afinidad por una amplia gama de micotoxinas (Biernasiak et al., 2006).
⇰ Se cree que la matriz de glucomanano del preparado MOS atrapa las micotoxinas de forma irreversible (Afzali y Devegowda, 1998).
⇰ Además, se supone que una pequeña porción de MOS modificada podría ser absorbida en el intestino delgado por las células M, provocando la activación de los linfocitos B y la subsiguiente activación de los linfocitos T y los macrófagos, lo que conduce a una mejora general del estado inmunitario de las aves (Savage et al., 1996).
La capacidad de fijación de micotoxinas de la MOS se ha demostrado en varios ensayos in vitro e in vivo (Stanley et al., 1993; Devegowda et al., 1996; Afzali y Devegowda, 1998; Devegowda et al., 1998; Raju y Devegowda, 2000; Swamy y otros, 2004; Yegani y otros, 2006; Awaad y otros, 2011; Fowler y otros, 2015; Farooqui y otros, 2019; Arif y otros, 2020).
CONCLUSIONES
|
Existe una amplia gama de adsorbentes de micotoxinas y agentes antifúngicos disponibles en el mercado con efectos de potencia variable para reducir la presencia o eliminar la toxicidad de las micotoxinas en los alimentos para avicultura. El desarrollo de un absorbente de micotoxinas comercial exitoso requiere la incorporación de lo mejor de estos ingredientes activos en la concentración requerida para asegurar una reducción general de los efectos dañinos de la presencia de micotoxinas en las dietas avícolas. |

BIBLIOGRAFÍA
Abdel-Wahhab, M.A., S.E. Aly. 2005. Antioxidant property of Nigella sativa (black cumin) and Syzygium aromaticum (clove) in rats during aflatoxicosis. J. Appl. Toxicol., 25: 218-223.
Arif, M., Iram, A., Bhutta, M., Naiel, M., Abd El-Hack, M. E., Othman, S. I., Allam, A. A., Amer, M. S., & Taha, A. E. 2020. The Biodegradation Role of Saccharomyces cerevisiae against Harmful Effects of Mycotoxin Contaminated Diets on Broiler Performance, Immunity Status, and Carcass characteristics. Animals: an open access journal from MDPI, 10(2), 238.
Awaad, M. H. H., A. M. Atta, Wafaa A. Abd El-Ghany, M. Elmenawey, K. Ahmed; A. A. Hassan, A. A. Nada and G. A. Abdelaleem. 2011. Effect of a Specific Combination of Mannan-Oligosaccharides and β-Glucans Extracted from Yeast Cell Wall on the Health Status and Growth Performance of Ochratoxicated Broiler Chickens. Journal of American Science, 7(3):82-96.
Afzali, N. and Devegowda, G., 1999. Ability of modified mannanoligosaccharide to counteract aflatoxicosis in broiler breeder hens. Poult. Sci. Abs., 229.
Alexandros Y, Jean PJ. 2002. Mycotoxins in feeds and their fate in animals. Asian Australasian Journal of Animal Sciences. 51:81-99.
Bata, Á., R. Lásztity. 1999. Detoxification of mycotoxin-contaminated food and feed by microorganisms. Trends Food Sci Technol, 10 (6):223-228.
Biernasiak J., Piotrowska M., Libudzisz Z. 2006. Detoxification of mycotoxins by probiotic preparation for broiler chickens. Institute of Fermentation Technology and Microbiology, Technical University of Lodz, Poland. Mycotoxin Research. 22(4): 230 235
Bryden, W.L. 2012. Mycotoxin contamination of the feed supply chain: Implications for animal productivity and feed security. Anim. Feed Sci. Technol. 173, 134–158.
Chaucheyras-Durand, F., F. Ossa. 2014. Review: The rumen microbiome: Composition, abundance, diversity, and new investigative tools. Prof. Anim. Sci., 30: 1-12.
Chow, C.K., 2001. Vitamin E regulation of mitochondrial superoxide generation. Biololgy of Signal Receptors, 10: 112-124.
Coelho, M., 1996. Optimum vitamin supplementation needed for turkey performance and profitability. Feedstaffs. 68: 13-21.
Daković A, Tomasević-Canović M, Dondur V, Rottinghaus GE, Medaković V, Zarić S. 2005. Adsorption of mycotoxins by organozeolites. Colloids Surf B Biointerfaces. 46(1):20-5. doi: 10.1016/j.colsurfb.2005.08.013. Epub 2005 Sep 28. PMID: 16198090.
Dhanasekaran, D. S. Shanmugapriya, N. Thajuddin, A. Panneerselvam. 2011. Aflatoxins and Aflatoxicosis in Human and Animals. Aflatoxins- Biochemistry and Molecular Biology, 221-254.
Dal Bosco, Z. Gerencsér, Z. Szendro, C. Mugnai, M. Cullere, M. Kovács, S. Ruggeri, S. Mattioli, C. Castellini, A. Dalle Zotte. 2014. Effect of dietary supplementation of Spirulina (Arthrospira platensis) and Thyme (Thymus vulgaris) on rabbit meat appearance, oxidative stability and fatty acid profile during retail display. Meat Sci., 96: 114-119
Dalleau S, Cateau E, Berges T, Berjeaud J, Imbert C. 2008. In vitro activity of terpenes against Candida biofilms International Journal of Antimicrobial Agents 31 572–576.
Devegowda, G., Aravind, B.I.R. and Morton, M.G. 1996. Saccharmyces cerevisiae and mannanoligosaccharides to counteract aflatoxicosis in broilers. In: Proc. Australian Poult. Sci. Symp., Sydney, Australia, 8: 103-106.
Devegowda, G., Raju, M.V.L.N. and Swamy, H.V.L.N. 1998. Mycotoxins: Novel solutions for their counteraction. feedstuffs. 70: (50): 12-16.
Diaz D.E, Smith TK. Mycotoxins sequestering agents: Practical tools for neutralization of mycotoxins. In: The Mycotoxin Blue Book. England: Nottingham University Press; 2005. pp. 323-339.
Ditta, Y.A., S. Mahad and U. Bacha 2018. Aflatoxins: Their Toxic Effect on Poultry and Recent Advances in Their Treatment, Mycotoxins – Impact and Management Strategies, Patrick Berka Njobeh and Francois Stepman, IntechOpen, Döll S., Dänicke S.2004. In vivo detoxification of fusarium toxins. Arch. Anim. Nutr. 58:419441.
Döll S., Dänicke S., Valenta H., Flachowsky G. 2004. In vitro studies on the evaluation of mycotoxin detoxifying agents for their efficacy on deoxynivalenol and zearalenone. Arch. Anim. Nutr. 58:311324.
Dvorak, M., 1989. Ability of bentonite and natural zeolite to adsorb aflatoxin from liquid media. Vet. Med. (Praha). 34: 733-741.
Duarte, E.D. and Smith, T.K. 2005. Mycotoxin blue book. Nottingham University press. pp. 323-339.
Edlayne G, Simone A, Felicio JD. 2009. Chemical and biological approaches for mycotoxin control: A review. Recent Patents on Food, Nutrition & Agriculture. 1(2):155-161.
EFSA FEEDAP Panel (EFSA Panel on Additives and Products or Substances used in Animal Feed), 2016. Safety and efficacy of a preparation of algae interspaced bentonite as a feed additive for all animal species. EFSA Journal, 14(11): 4623-4638.
Egbontan AO, Afolabi CG, Kehinde IA, Enikuomehin OA, Ezekiel CN, Sulyok M, Warth B, Krska R. 2017. A mini-survey of moulds and mycotoxins in locally grown and imported wheat grains in Nigeria. Mycotoxin Res., 33(1):59-64.
Ehrich, M., Driscoll, C. and Larsen, C., 1986. Ability of ethoxiquin and butylated hydroxytoluene to counteract deleterious effects of dietary aflatoxin in chicks. Avian Dis., 30: 802-807.
Eralsan, G., Essz, D., Akdogan, M., Sahindokuyucu, F. and Altrintas, L., 2005. The effects of aflatoxin and sodium bentonite and alone on some blood electrolyte levels in broiler chickens. Turk Veterinerlik ve Hayvanclk Dergisi. 29: 601-605.
Eralson, G., Essz, D., Akdogan, M., Karoz, E., Oncu, M. and Ozyldz, Z., 2006. Efficacy of dietary sodium bentonite against subchronic exposure to dietary aflatoxin in broilers. Bulletin of the veterinary Institute in Puawy. 50: 107-112.
Fan, Y., Lihong Zhao, Qiugang Ma, Xiaoying Li, Huiqin Shi, Ting Zhou, Jianyun Zhang, Cheng Ji, 2013. Effects of Bacillus subtilis ANSB060 on growth performance, meat quality and aflatoxin residues in broilers fed moldy peanut meal naturally contaminated with aflatoxins Food Chem Toxicol, 59: 748-753.
Fan, Y.; Zhao, L.; Ji, C.; Li, X.; Jia, R.; Xi, L.; Zhang, J.; Ma, Q. 2015. Protective Effects of Bacillus subtilis ANSB060 on Serum Biochemistry, Histopathological Changes and Antioxidant Enzyme Activities of Broilers Fed Moldy Peanut Meal Naturally Contaminated with Aflatoxins. Toxins 7, 3330-3343.
Farooqui M., Khalique A., Rashid M., Mehmood S., Malik M. 2019. Aluminosilicates and yeast-based mycotoxin binders: Their ameliorated effects on growth, immunity and serum chemistry in broilers fed aflatoxin and ochratoxin. S. Afr. J. Anim. Sci. 49:619–627.
Fowler J, Wei L, Christopher B. 2015. Effects of a calcium bentonite clay in diets containing aflatoxin when measuring liver residues of aflatoxin B1 in starter broiler chicks. Toxins. 7(9):3455-3464.
Fruhauf, S.; Novak, B.; Nagl, V.; Hackl, M.; Hartinger, D.; Rainer, V.; Labudova, S.; Adam, G.; Aleschko, M.; Moll, W.D. 2019. Biotransformation of the mycotoxin zearalenone to its metabolites hydrolyzed zearalenone (HZEN) and decarboxylated hydrolyzed zearalenone (DHZEN) diminishes its estrogenicity in vitro and in vivo. Toxins 11, 481.
Ganesan, A.R., Balasubramanian, B., Park, S. Jha, R., Andretta, I., Bakare, A.G., Kim, I.H. 2021. Ochratoxin A: Carryover from animal feed into livestock and the mitigation strategies. Animal Nutrition, 7(1): 56-63.
Garai, E.; Risa, A.; Varga, E.; Cserháti, M.; Kriszt, B.; Urbányi, B.; Csenki, Z. 2021. Evaluation of the Multimycotoxin-Degrading Efficiency of Rhodococcus erythropolis NI1 Strain with the Three-Step Zebrafish Microinjection Method. Int. J. Mol. Sci. 22:724.
Girish, C.K., and Devegowda, G., 2004. Evaluation of modified glucomannan (Mycosorb) and HSCAS to ameliorate the individual and combined toxicity of aflatoxin and T-2 toxin in broiler chickens. In: Aust. Poult. Sci. Symp. 16: 126-129. Sydney, Australia.
Gowda, N.K.S. and Ledoux, D.R., 2008. Use of antioxidants in amelioration of mycotoxin toxicity: a review. Anim. Nutr. Food Tech., 8: 1-11.
Gowda, N.K.S., Ledoux, D.R., Rottinghaus, G.E., Bermudez, A.J. and Chent, Y.C., 2008. Efficacy of Turmeric (Curcuma longa), containing a known level of Curcumin, and Hydrated Sodium Calcium Aluminosilicates to ameliorate the adverse effects of aflatoxin in broiler chicks. Poult. Sci., 87:1125-1130.
Hahn, I.; Kunz-Vekiru, E.; Twaruzek, M.; Grajewski, J.; Krska, R.; Berthiller, F. 2015. Aerobic and anaerobic in vitro testing of feed additives claiming to detoxify deoxynivalenol and zearalenone. Food Addit. Contam. Part A. 32, 922–933.
Hagler, W.M., Grimes, JR., J.L. and Fairchild., 1992. Effects of Astra-Ben 20® on broiler chicks exposed to AFB1 or T-2 toxin. North Carolina State University. Poult. Abstr., 16: 123.
Haschek WM, Voss KA, Beasley VR. 2002. Selected Mycotoxins Affecting Animal and Human Health. 2nd ed. Vol. 1. New York: Academic Press; pp. 645-699.
Hoehler, D. and Marquardt, R.R., 1996. Influence of vitamin E and C on the toxic effects of ochratoxin A and T-2 toxin in chicks. Poult. Sci., 75: 1508-1515.
Huff, W.E., Kubena, L.F., Harvey, R.B. and Phillips, T.D., 1992. Efficacy of hydrated sodium calcium aluminosilicate to reduce the individual and combined toxicity of aflatoxin and ochratoxin A. Poult. Sci., 71: 64-69.
Hussein, H.S., J.M. Brasel. 2001. Toxicity, metabolism and impact of mycotoxins on humans and animals. Toxicology, 167: 101-134.
Huwing A., Freimund S., Käppeli O. and Dutler H. 2001. Mycotoxin detoxication of animal feed by different adsorbents. Toxicology Letters. 122(2): 179-188.
Iqbal, Q.K., Rao, P.V. and Reddy, S.J., 1983. Dose-response relationship of experimentally induced aflatoxicosis in commercial layers. Indian J. Anim. Sci., 53: 1277-1280.
Jaynes W.F., Zartman R.E., Hudnall W.H. 2007. Aflatoxin B1 adsorption by clays from water and corn meal. Applied Clay Science, 36(1-3):197-205.
Ji, C.; Fan, Y.; Zhao, L. 2016. Review on biological degradation of mycotoxins. Anim. Nutr., 2: 127–133.
Jindal, N., Mahipal, S.K. and Mahajan, N.K., 1993. Effect of hydrated sodium calcium aluminosilicate on prevention of aflatoxicosis in broilers. Indian J. Anim. Sci., 63: 649-652.
Johri, T.S., Agrawal, R. and Sadagopan, V.R., 1990. Effects of low dietary levels of aflatoxin on laying quails (Coturnix coturnix japonica) and their response to dietary modifications. Indian J. Anim. Sci., 60: 355-359.
Jouany, J.P., A. Yiannikouris, G. Bertin. 2009. Risk assessment of mycotoxins in ruminants and ruminant products Options Mediterranéennes A, 85: 205-224.
Kabak, B.; Dobson, A.D.; Var, I. 2006. Strategies to prevent mycotoxin contamination of food and animal feed: A review. Crit. Rev. Food Sci. Nutr., 46: 593–619.
Kabak B. 2009. The fate of mycotoxins during thermal food processing. Journal of the Science of Food and Agriculture.89:549-554.
Kagan, V.E. and Tyurina, Y.Y.. 1998. Recycling and redox cycling of phenolic antioxidants. Towards orolongation of the healthy life span. Annals of New York Academy of Sciences, 854: 425-434.
Kiessling, K.H., Petersson, H., Sandholm, K. and Olsen, M. 1984. Metabolism of aflatoxin, ochratoxin, zearalenone and three trichothecenes by intact rumen fluid, rumen protozoa and rumen bacteria. Appl. Env. Microbiol., 47: 1070-1073.
Kolossova A, Stroka J. 2009. Evaluation of the effect of mycotoxin binders in animal feed on the analytical performance of standardised methods for the determination of mycotoxins in feed. 29(12): 1959-1971.
Kong, Q.; Zhai, C.; Guan, B.; Li, C.; Shan, S.; Yu, J. 2012. Mathematic Modeling for Optimum Conditions on Aflatoxin B1 Degradation by the Aerobic Bacterium Rhodococcus erythropolis. Toxins. 4: 1181-1195.
Khatoon A, Khan MZ, Abidin ZU, Bhatti SA. 2018. Effects of feeding bentonite clay upon ochratoxin A induced immunosuppression in broiler chicks. Food Addit Contam A. 35(3): 538e45.
Krska, R.; Schubert-Ullrich, P.; Molinelli, A.; Sulyok, M.; MacDonald, S.; Crews, C. 2008, Mycotoxin analysis: An update. Food Addit. Contam. Part A 25, 152–163.
Kubena L. F., Harvey R. B., Bailey R. H., Buckley S. A., and Rottinghaus G. E. 1998. Effects of a Hydrated Sodium Calcium Aluminosilicate (T-Bindä) on Mycotoxicosis in Young Broiler Chickens. Poultry Science 77: 1502–1509
Kusumaningtyas E, Widiastuti R, Maryam R. 2006. Reduction of aflatoxin B1 in chicken using Saccharomyces cerevisiae, Rhizopus and their combination. Mycopathologia. 162(4): 307-311.
Lahtinen SJ, Haskard CA, Ouwehandz AC, Salminenz SJ, Ahokasy JT. 2004. Binding of aflatoxin B1 to cell wall components of Lactobacillus rhamnosus strain GG. Food Additives and Contaminants. 21(2): 158-164.
Lee, S.E., Campbell, B.C., Russel, J., Molyneux., Hasegawa, S. and Lee, H.S., 2001. Inhibitory effects of naturally occurring compounds on aflatoxin B1 biotransformation. J. Agri. Food Chem., 49: 5171-5177.
Linderfelser, L.A. and Ciegler, A., 1970. Studies on aflatoxin detoxification in shelled corn by ensiling. J. Agri. Food Chem. 18: 640-643.
Ma, Q.G., X. Gao, T. Zhou, L.H. Zhao, Y. Fan, X.Y. Li, Y.P. Lei, C. Ji, J.Y. Zhang, 2012. Protective effect of Bacillus subtilis ANSB060 on egg quality, biochemical and histopathological changes in layers exposed to aflatoxin B1 Poult Sci, 91(11): 2852-2857
Manafi, M., B. Umakantha, H. D. Narayana Swamy and K. Mohan 2009. Evaluation of High-Grade Sodium Bentonite on Performance and Immune Status of Broilers, Fed Ochratoxin and Aflatoxin. World Mycotoxin Journal. 2(4): 435-440.
Manafi, M. 2011. Evaluation of Different Mycotoxin Binders on Broiler Breeders Induced with Aflatoxin B1: Effects on Biochemical and Immunological Parameters. Research Journal of Fisheries and Hydrobiology, 6(4): 445-450.
Manafi, M., K. Mohan, and M. Noor Ali. 2011. Effect of Ochratoxin A on Coccidiosis Challenged Broiler Chicks. World Mycotoxin Journal. 4(2): 177-181.
Manafi, M., H.N.N. Murthy and H.D. Narayana Swamy. 2012. Evaluation of Different Mycotoxin Binders on Broiler Breeders Induced With Aflatoxin B1: Effects on Visceral Organ Weight and Organ Lesions Parameters. American-Eurasian Journal of Agricultural & Environmental Sciences. 12 (5):574-578.
Manafi, M., M. Hedayati and M. Yari. 2014. Effectiveness of Rosemary (Rosmarinus officinalis L.) Essence on Performance and Immune Parameters of Broilers during Aflatoxicosis. Advances in Life Sciences, 4(3): 166-173.
Manafi, M., H. Arak and Hedayati, M. 2015. The effects of inclusion of various levels of aflatoxin B1 on performance, relative weights of internal organs and blood parameters of Japanese quail during the growing period (1-28 days). Animal Science Journal, 107:33-40.
Manafi, M. and M. Hedayati. 2016. Combinational Effects of Thyme and Rosemary Ethanolic Extractions in Reducing the Effects of Aflatoxin B1 in Broilers. Animal Science Journal, 112: 105-116.
Manafi, M. 2018. Toxicity of aflatoxin B1 on laying Japanese quails (Coturnix coturnix japonica). Journal of Applied Animal Research. 46(1):953-959.
Manafi, M., M. Hedayati, N. Pirany and Omede Apeh Akwu. 2019. Comparison of performance and feed digestibility of the non-antibiotic feed supplement (Novacid) and an antibiotic growth promoter in broiler chickens. Poultry Science. 98(2): 904-911.
Marin, S.; Ramos, A.J.; Cano-Sancho, G.; Sanchis, V. 2013. Mycotoxins: Occurrence, toxicology, and exposure assessment. Food Chem. Toxicol. 60:218–237.
May, J.M., Cobb, C.E., Mendriratta, S., Hill, K.E. and Burk, R.F. 1998. Reduction of ascorbyl free radical to ascorbate by thioredoxin reductase. J. Bio. Chem., 273: 23039-23045.
Mgbeahuruike, A.C., Tochukwu E. Ejioffor, Obasi C. Christian, Vincent C. Shoyinka, Magnus Karlsson, Erik Nordkvist. 2018. Detoxification of Aflatoxin-Contaminated Poultry Feeds by 3 Adsorbents, Bentonite, Activated Charcoal, and Fuller’s Earth, Journal of Applied Poultry Research, 27(4): 461-471.
Mishra, S., K.M. Ansari, P.D. Dwivedi, H.P. Pandey, M. Das. 2013. Occurrence of deoxynivalenol in cereals and exposure risk assessment in Indian population. Food Control. 30(2): 549-555.
Murugesan, G.R.; Ledoux, D.R.; Naehrer, K.; Berthiller, F.; Applegate, T.J.; Grenier, B.; Phillips, T.D.; Schatzmayr, G. 2015. Prevalence and effects of mycotoxins on poultry health and performance, and recent development in mycotoxin counteracting strategies. Poult. Sci. 94: 1298–1315.
Nyandieka, H.S., Wakhis, J. and Kilonzo, M.M., 1990. Association of reduction of AF B1–induced liver tumors by antioxidants with increased activity of microsomal enzymes. Indian J. Med. Res., 92: 332-336.
Murugesan, G.R., D.R. Ledoux, K. Naehrer, F. Berthiller, T.J. Applegate, B. Grenier, T.D. Phillips, G. Schatzmayr, 2015. Prevalence and effects of mycotoxins on poultry health and performance, and recent development in mycotoxin counteracting strategies. Poultry Science, 94(6):1298-1315.
Newbold, C.J., G. de la Fuente, A. Belanche, E. Ramos-Morales, N. McEwan. 2015. The role of ciliate protozoa in the rumen Front. Microbiol., 6:1313
Niderkorn V., Morgavi D.P., Pujos E., Tissandier A., Boudra H. 2007. Screening of fermentative bacteria for their ability to bind and biotransform deoxynivalenol, zearalenone and fumonisins in an in vitro simulated corn silage model. Food Additives and Contaminants, 24: 406-415.
Park, J.H., S.I. Lee, I.H. Kim. 2018. Effect of dietary Spirulina (Arthrospira) platensis on the growth performance, antioxidant enzyme activity, nutrient digestibility, cecal microflora, excreta noxious gas emission, and breast meat quality of broiler chickens. Poultry Science, 97(7):2451-2459.
Pasteiner, S. 1997. Copying with mycotoxin contaminated feed stuffs. Feed Int., 18: 12-16.
Phillips, T.D., Kubena, L.F., Harvey, R.B., Taylor and Heidelbaugh, N.D. 1988. Hydrated sodium calcium aluminosilicate: a high affinity sorbent for aflatoxin. Poult. Sci., 67: 243-247.
Raj, J., M. Vasiljević, P. Tassis, H. Farkaš, J. Bošnjak-Neumüller & K. Männer. 2021. Effects of a modified clinoptilolite zeolite on growth performance, health status and detoxification of aflatoxin B1 and ochratoxin A in male broiler chickens, British Poultry Science. Mar 12: 1-10.
Raj J, Vasiljević M, Tassis P, Farkaš H, Bošnjak-Neumüller J, Männer K. 2021. Effects of a modified clinoptilolite zeolite on growth performance, health status and detoxification of aflatoxin B1 and ochratoxin A in male broiler chickens. Br Poult Sci. 12:1-10. doi:10.1080/00071668.2021.1891522. Epub ahead of print. PMID: 33595390.
Rajendran RM, Umesh B, Chirakkal H. 2020. Assessment of H-bzeolite as an ochratoxin binder for poultry. Poultry Sci. 99: 76-88.
Raju M.V.L.N., Devegowda G. 2000. Influence of esterifield-glucomannan on performance and organ morphology, serum biochemistry and haematology in broilers exposed to individual and combined mycotoxicosis (aflatoxin, ochratoxin and T-2 toxin). Brit Poultry Sci 41: 640-650.
Raju, M.V.L.N., Rama Rao, S.V., Radhika, K. and Chawak, M.M. 2004. Effects of spirulina platensis or furazolidone on the performance and immune response of broiler chickens fed with aflatoxin contaminated diet. Indian J. Anim. Nutr. 21: 40-44.
Ramos A.J., Hernandez E., PlaDelfina J.M., Merino M. 1996. Intestinal absorption of zearalenone and in vitro study of non-nutritive sorbent materials. Int. J. Pharm. 128:129137.
Rawal S, Ji EK, Roger C. 2010. Aflatoxin B1in poultry: Toxicology, metabolism and prevention. Research in Veterinary Science. 89(3): 325-331.
Renzulli, C., Galvano, F., Pierdomenico, L., Speroni, E. and Guerra, M.C. 2004. Effects of Rosamarinic acid against aflatoxin B1 and ochratoxin A induced cell damage in a human hepatoma cell line. J. Appli. Toxico., 24: 289-296.
Rosa, C.A.R., Miazoo, R., Magnoli, C., Salvano, M., Chicchiera, S.M., Ferrero, S., Saenz, M. Carvalho, E.C.Q., and Dalcero, A. 2001. Evaluation of the efficacy of bentonite from the south Argentina to ameliorate the toxic effects of aflatoxin in broilers. Janerio Institute de Veterrinaria, Brazil.
Ruan D, Wang WC, Lin CX, Fouad AM, Chen W, Xia WG, Zheng CT. 2019. Effects of curcumin on performance, antioxidation, intestinal barrier and mitochondrial function in ducks fed corn contaminated with ochratoxin A. Animal. 13(1): 42-52.
Santurio, J.M., Mallmannl, C.A., Rosa, A.P., Appel, G., Heer, A., Dageforde, S. and Bottcher, M., 1999. Effect of sodium bentonite on the performance and blood variables of broiler chickens intoxicated with aflatoxin. Br. Poult. Sci., 40: 115-119.
Savage, T.F., Cotler, P.F. and Zakrzewska, E.I. 1996. The effect of feeding mannanoligosaccharide on immunoglobulins, plasma IgG and bile IgA of World stad MW male turkeys. Poult. Sci., 75: 143.
Smith, J.E. and Ross, K. 1991. The toxigenic Aspergilli. In: Mycotoxins and Animal Foods, Eds: J.E. Smith and Henderson, CRC Press, Boca Raton, pp. 101-118.
Solfrizzo M., Visconti A., Avantaggiato G., Torres A., Chulze S. 2001. In vitro and in vivo studies to assess the effectiveness of cholestyramine as a binding agent for fumonisins. Mycopathologia 151:14753.
Stanley, V.G., Ojo, R., Woldensenbet, S. and Hutchinson, D.H. 1993. The use of Saccharmyces cerevisiae to suppress the effects of aflatoxicosis in broiler chicks. Poult. Sci., 72: 1867-1872.
Surai, P.F., 2001. Natural antioxidants in avian nutrition and reproduction. 1st ed. Nottingham University press, U.K.
Swamy, H.V.L.N., Smith, T.K., Karrow, N.A. and Boermans, H.J. 2004. Effects of feeding blends of grains naturally contaminated with Fusarium mycotoxins on growth and immunological parameters of broiler chickens. Poult. Sci., 83: 533-543.
Tso, Ko-Hua; Ju, Jyh-Cherng; Fan, Yang-Kwang; Chiang, Hsin-I. 2019. “Enzyme Degradation Reagents Effectively Remove Mycotoxins Deoxynivalenol and Zearalenone from Pig and Poultry Artificial Digestive Juices” Toxins 11(10):599. https://doi.org/10.3390/toxins11100599
Turbic A, Ahokas JT, Haskard CA. 2002. Selective in vitro binding of dietary mutagens, individually or in combination, by lactic acid bacteria. Food Additives and Contaminants.19: 144-152.
Unsworth, E.F., Pearce, J., Mcmurray, C.H., Moss, B.W., Gordon, F.J. and Rice, D., 1989. Investigations of the use of clay minerals and Prussian blue in reducing the transfer of dietary radiocesium to milk. Sci. Total Environ., 85: 339–347.
Upadhaya, S.D., M.A. Park, J.K. Ha. 2010. Mycotoxins and their biotransformation in the rumen: A review J. Anim. Sci. 23: 1250-1260.
Vekiru, E.; Hametner, C.; Mitterbauer, R.; Rechthaler, J.; Adam, G.; Schatzmayr, G.; Krska, R.; Schuhmacher, R. 2010. Cleavage of zearalenone by Trichosporon mycotoxinivorans to a novel nonestrogenic metabolite. Appl. Environ. Microbiol. 76:2353–2359.
Verma, R.J. and Nair, A., 2004. Ameliorative effect of vitamin E on aflatoxin induced lipid peroxidation in the testes of mice. Asian J. Andrololgy, 3: 217-221.
Vieira, S.L., 2003. Nutritional implication of mould development in feed stuffs and alternatives to reduce the mycotoxin problem in poultry feeds. World’s Poult. Sci. J., 59: 111-122.
Wei, J. T., Wu, K. T., Sun, H., Khalil, M. M., Dai, J. F., Liu, Y., Liu, Q., Zhang, N. Y., Qi, D. S., & Sun, L. H. 2019. A Novel Modified Hydrated Sodium Calcium Aluminosilicate (HSCAS) Adsorbent Can Effectively Reduce T-2 Toxin-Induced Toxicity in Growth Performance, Nutrient Digestibility, Serum Biochemistry, and Small Intestinal Morphology in Chicks. Toxins, 11(4): 199. https://doi.org/10.3390/toxins11040199.
Weiss, W.P., 2002. Amntioxidants nutrients and milk quality. In: Roche symposium, pacific Northwest nutrition conference, Vancouver, British Columbia, Canada.
Wu, Q., A. Jezkova, Z. Yuan, L. Pavlikova, V. Dohnal, K. Kuca. 2009. Biological degradation of aflatoxins Drug Metab Rev, 41 (1): 1-7.
Yegani, M., Smith, T. K., Leeson, S. and Boermans, H. J., 2006. Effects of Feeding Grains Naturally Contaminated with Fusarium Mycotoxins on Performance and Metabolism of Broiler Breeders. Poult. Sci., 85: 1541-1549.




 Prevención de micotoxicosis
Prevención de micotoxicosis